Ortokarbonata acido
| Ortokarbonata acido | ||
| Kemia formulo | ||
 | ||
Ortokarbonata acido | ||
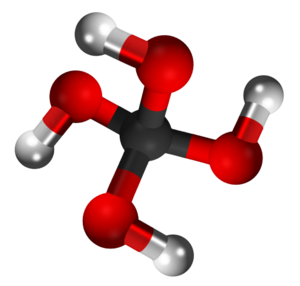 | ||
| Alternativa(j) nomo(j) | ||
| ||
| CAS-numero-kodo | 463-84-3 | |
| ChemSpider kodo | 7826887 | |
| PubChem-kodo | 9547954 | |
| Fizikaj proprecoj | ||
| Aspekto | travidebla oleeca likvaĵo[2] | |
| Molmaso | 80,04036g mol−1 | |
| Denseco | 1,276 g/cm−3[3] | |
| Fandpunkto | 83,9°C [4] | |
| Bolpunkto | 210°C | |
| Refrakta indico | 1,6490 | |
| Ekflama temperaturo | 36,9°C | |
| Solvebleco | Akvo:malmulte solvebla Solvebla en kloroformo, etila cetato kaj metanolo. | |
| Mortiga dozo (LD50) | >2000 mg/kg (buŝe) | |
| GHS etikedigo de kemiaĵoj | ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H225, H315, H319, H335 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264+265, P272, P280, P302+352, P305+354+338, P317, P321, P333+313, P362+364, P501 | |
(25 °C kaj 100 kPa) | ||
Ortokarbonata acido aŭ ortokarbonata acido estas organika kombinaĵo rezultanta el hidrolizo de la trikloronitrilo'. Ĝi estas travidebla oleeca likvaĵo, nesolvebla en akvo. Ortokarbonata acido posedas 1 karbonatomon, 4 hidrogenatomojn, kaj 4 oksigenatomojn. Ortokarbonata acido uzatas en kemiaj sintezoj kaj en la preparado de karbonataĵoj kaj ortokarbonataj derivaĵoj. Ĝia molekula strukturo konsistas el ununura karbonatomo ligita al kvar hidroksilaj grupoj. Estus do kvarobla alkoholo. Eblas, ke la kernoj de Neptuno kaj Urano povas enhavi signifajn kvantojn de polimero de karbonata acido kaj ortokarbona acido,” diras la rusa kemiisto Artem Oganov. Poliortokarbonatoj estas stabilaj polimeroj kiuj povas havi aplikojn en la sorbado de organikaj solvantoj en procezoj de rubaĵo-traktadoj aŭ en dentaj restaŭraj materialoj. Ortokarbonatoj estas malstabilaj en acida medio kaj stabilaj en alkala medio.

Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
- Preparado de la ortokarbonata acido per traktado de karbona tetraklorido kaj kupra (II) hidroksido:[5]
Sintezo 2[redakti | redakti fonton]
- Preparado de la ortokarbonata acido per traktado de karbona tetraklorido kaj kupra (I) hidroksido:
Sintezo 3[redakti | redakti fonton]
- Preparado de la fenila ortokarbonato per traktado de fenolo kaj karbona tetraklorido:
Sintezo 4[redakti | redakti fonton]
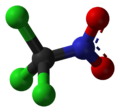
- Preparado de la ortokarbonata acido per hidrolizo de la trikloroacetonitrilo:
Sintezo 5[redakti | redakti fonton]
- Preparado de la ortokarbonata acido per hidrolizo de la kloropikrino:
Vidu ankaŭ[redakti | redakti fonton]
Referencoj[redakti | redakti fonton]
- ↑ Moscow Institute of Physics and Technology. Arkivita el la originalo je 2022-12-05. Alirita 2023-04-23.
- ↑ Toronto Research Chemicals
- ↑ GuideChem
- ↑ EPA United States Environmental Protection Agency
- ↑ Comprehensive Organic Functional Group Transformations





![{\displaystyle {\mathsf {{\xrightarrow[{}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/af21b07e9e503bdbbee6814c136975f68f374663)