Nitrofenilacetata acido
Etoso
| p-Nitrofenilacetata acido | ||
 | ||
| Plata kemia strukturo de la Nitrofenilacetata acido | ||
 | ||
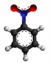
| Tridimensia kemia strukturo de la Nitrofenilacetata acido | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 104-03-0 | |
| ChemSpider kodo | 4500 | |
| PubChem-kodo | 4661 | |
| Merck Index | 15,6709 | |
| Fizikaj proprecoj | ||
| Aspekto | blanka solidaĵo | |
| Molmaso | 181,15 g·mol-1 | |
| Denseco | 1,4283g cm−3 | |
| Fandpunkto | 150°C-155°C[1] | |
| Bolpunkto | 377,6°C[2] | |
| Refrakta indico | 1,5468 | |
| Ekflama temperaturo | 171,6 °C[3] | |
| Acideco (pKa) | 3,85 | |
| Solvebleco | Akvo:3,57 g/L [4] | |
| Mortiga dozo (LD50) | 489 mg/kg (buŝe) | |
| Sekurecaj Indikoj | ||
| Riskoj | R36/37/38 | |
| Sekureco | S26 S36 S37/39 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P321, P332+313, P337+313, P362, P403+233, P405, P501[5] | |
(25 °C kaj 100 kPa) | ||
Nitrofenilacetata acido aŭ C8H7NO4 estas organika aromata kombinaĵo apartenanta al la familio de la acidoj. Nitrofenilacetata acido estas flava solidaĵo malmulte solvebla en malvarma akvo sed solvebla en etanolo, duetila etero kaj benzeno. Ĝi estas grava ingredienco kaj peraĵo uzata en organikaj sintezoj kun medicinaj proprecoj. Ĝi estiĝas per hidrolizo de la "p-nitrofenilacetonitrilo", varmigante kaj refluigante miksaĵon da p-nitrofenilacetonitrilo, sulfata acido kaj akvo dum 15 minutoj. Nitrofenilacetata acido estas uzata en farmaciaj industrioj kaj en la produktado de aliaj organikaj sintezoj.
Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
- Preparado ekde la nitrobenzila cianido[6]:
Sintezo 2[redakti | redakti fonton]
- Preparado ekde la nitrobenzaldehido kaj karbona unuoksido:
Sintezo 3[redakti | redakti fonton]
- Preparado ekde la nitrobenzila alkoholo:
Sintezo 4[redakti | redakti fonton]
- Preparado ekde la nitrofenolo:
Sintezo 5[redakti | redakti fonton]
- Preparado ekde la benzaldehido:
Sintezo 6[redakti | redakti fonton]
- Preparado ekde la benzila cianido:
Sintezo 7[redakti | redakti fonton]
- Preparado ekde la fenilacetata acido:
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- Konvertado al nitrobenzila cianido:
Reakcio 2[redakti | redakti fonton]
- Konvertado al nitrobenzaldehido:
Reakcio 3[redakti | redakti fonton]
- Konvertado al nitrobenzila alkoholo:
Reakcio 4[redakti | redakti fonton]
- Konvertado al nitrofenolo:
Reakcio 5[redakti | redakti fonton]
- Konvertado al benzaldehido:
Reakcio 6[redakti | redakti fonton]
- benzila cianido:
Reakcio 7[redakti | redakti fonton]
- Konvertado al fenilacetata acido:
Literaturo[redakti | redakti fonton]
- Taylor & Francis online
- Drugbank
- Chemistry of Penicillin
- Essential Principles of Organic Chemistry
- Purification of Laboratory Chemicals
- Essential Principles of Organic Chemistry
- Biochemistry
- Advances in Physical Organic Chemistry





![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)


![{\displaystyle {\mathsf {{\xrightarrow[{-H_{2}O}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f43b576bd9ed502188c0c051352bf946467a579c)
![{\displaystyle {\mathsf {{\xrightarrow[{-CO_{2}}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b1078f5d8571a380da85494e6f89252d40a7d398)

![{\displaystyle {\mathsf {{\xrightarrow[{KMnO_{4}}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5a7ac55e3b8ca24b2281fc9784186a1a7d2e2eb7)
![{\displaystyle {\mathsf {{\xrightarrow[{-HCl}]{+Cl_{2}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/46b351306c8b813c77a2466699f112a2e5407450)
![{\displaystyle {\mathsf {{\xrightarrow[{-HCl}]{+HCN}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b9e6ac2172f3d86d8e736297f8971a5fe4efcc21)
![{\displaystyle {\mathsf {{\xrightarrow[{-H_{2}O}]{KMnO_{4}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/34ed78403a1ffbe958db13eaf3cbfca94b06113c)

![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{+KMnO_{4}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/affacfa8dbf74158abfd6848f8a83fe5fe8dbe4b)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{KMnO_{4}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e0eec0509b34cb7b5a3cd9270769fae6208ceaed)
![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{LiAlH_{4}}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7663c37c9a24e207e64cd3932d04346894c67fb0)