Buterila klorido
(Alidirektita el Butirila klorido)
| Buterila klorido | |||
 | |||
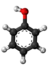
| Plata kemia strukturo de la Buterila klorido | |||
 | |||
| Tridimensia kemia strukturo de la Buterila klorido | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | |||
| CAS-numero-kodo | 141-75-3 | ||
| ChemSpider kodo | 8523 | ||
| PubChem-kodo | 8855 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora likvaĵo kun penetranta odoro | ||
| Molmaso | 106,549 g·mol-1 | ||
| Denseco | 1,026g cm−3[1] | ||
| Fandpunkto | -89°C[2] | ||
| Bolpunkto | 102°C[3] | ||
| Refrakta indico | 1,412 | ||
| Ekflama temperaturo | 18 °C | ||
| Solvebleco | Akvo:reakcias | ||
| Mortiga dozo (LD50) | >2000 mg/kg (buŝe) | ||
| Sekurecaj Indikoj | |||
| Riskoj | R11 R34 | ||
| Sekureco | S1 S2 S25 S36/37/39 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Damaĝa substanco | ||
| GHS Deklaroj pri damaĝoj | H225, H302, H314, H318, H331 | ||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P260, P264, P280, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P321, P363, P370+378, P403+235, P405, P501[4] | ||
(25 °C kaj 100 kPa) | |||
Buterila klorido aŭ C4H7ClO estas kemia kombinaĵo, apartenanta al la funkcia grupo de la halogenidoj de la buterata acido kaj kloro. Buterila klorido estas senkolora likvaĵo kun penetranta odoro, uzata kiel kemia reakciaĵo kaj en la fabrikado de kosmetikaĵoj kaj farmaciaĵoj. Kutime ĝi estiĝas per kondensiĝa reakcio aŭ per esterigo de Fischer-Speyer kun sulfata acido kiel katalizilo. Buterila klorido estas malmulte solvebla en akvo, sed tute solvebla en alkoholo, duetila etero, kloroformo kaj plejmulto el la organikaj solvantoj. Buterila klorido reakcias kun fortaj oksidigagentoj kaj fortaj bazoj kaj posedas antifungajn kaj antibakteriajn proprecojn.
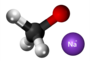
| Bonvolu ne konfuzi... | |
 |
 |
| Ili ne estas izomeroj sed apartenas al la sama klaso de la kloridoj, la unua posedas simplan ligilon en la tria karbono kaj la dua posedas duoblan ligilon en la tria karbono. | |
Sintezoj[redakti | redakti fonton]
Sintezo 1[redakti | redakti fonton]
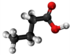
- Preparado per interagado de buterata acido kaj fosfora triklorido:
Sintezo 2[redakti | redakti fonton]
- Preparado kun buterata anhidrido kaj fosfora triklorido:
Sintezo 3[redakti | redakti fonton]
- Preparado per interagado de buterata acido kaj sulfurila klorido:
Sintezo 4[redakti | redakti fonton]
- Preparado per reakcio inter tionila klorido kaj buterata acido:
Sintezo 5[redakti | redakti fonton]
- Preparado per reakcio inter buterata acido kaj fosforila klorido:
Sintezo 6[redakti | redakti fonton]
- Preparado per reakcio inter buterata acido kaj okzalila klorido:
Sintezo 7[redakti | redakti fonton]
- Preparado per reakcio inter kalcia buterato kaj sulfurila klorido:
Reakcioj[redakti | redakti fonton]
Reakcio 1[redakti | redakti fonton]
- Reakcio kun natria hidroksido:
Reakcio 2[redakti | redakti fonton]
- Reakcio kun akvo:
Reakcio 3[redakti | redakti fonton]
- Reakcio kun fenolo:
Reakcio 4[redakti | redakti fonton]
- Reakcio kun natria metoksido:
Reakcio 5[redakti | redakti fonton]
- Reakcio kun etanolo:
Reakcio 6[redakti | redakti fonton]
- Reakcio kun arĝenta nitrito:
Reakcio 7[redakti | redakti fonton]
- Reakcio kun amoniako:
Reakcio 8[redakti | redakti fonton]
- Reakcio kun etilamino:
Literaturo[redakti | redakti fonton]
- Stenutz
- Parchem
- Toxic substances control act
- Qualitative Organic Microanalysis: Cognition and Recognition of Carbon Compounds
- Advances in Heterocyclic Chemistry
- The Dictionary of Substances and Their Effects
- Principles of Medicinal Chemistry
- Organic Chemistry: Aliphatic Compounds
Referencoj[redakti | redakti fonton]
- ↑ Sigma Aldrich[rompita ligilo]
- ↑ Chemical Book
- ↑ Chemicalland21
- ↑ PubChem





![{\displaystyle {\mathsf {{\xrightarrow[{\,}]{}}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a133815724e6bf6cfb39eb43f1e6c1d96ea8d17)